Libreta de apuntes
Enlaces relacionados
- Aceto balsámico
- Ácido acético
- Ácido ascórbico
- Ácido bórico
- Ácido butírico
- Ácido cafeico
- Ácido cítrico
- Ácido etanoico
- Ácido fólico
- Ácido fórmico
- Ácido fosfórico
- Ácido láctico
- Ácido málico
- Ácido metanoico
- Ácido propanoico
- Ácido sórbico
- Ácido tartárico
- Ácidos orgánicos
- Aditivos alimentarios
- Alcohol
- Alcohol etílico
- Bacterias lácticas
- Conservas caseras
- Cerveza
- Etanol
- Etileno
- Fermentación
- Fermentación acética
- Fermentación alcohólica
- Fermentación butírica
- Fermentación láctica
- Fermentación maloláctica
- Levadura
- Levadura química
- Metanol
- Recetas de cocina
- Sidra
- Vinagre
- Vino
ÍNDICE
La página de Bedri
|
ETILENO |
|
|
|
|
|
Nombre (IUPAC) sistemático |
|
|
Eteno |
|
|
General |
|
|
Fórmula semidesarrollada |
CH2=CH2 |
|
Fórmula molecular |
|
|
Identificadores |
|
|
Número CAS |
74-85-1 |
|
Propiedades físicas |
|
|
Estado de agregación |
Gas |
|
Apariencia |
Incoloro |
|
Densidad |
567 kg/m3; 0,567 g/cm3 |
|
Densidad del vapor |
0,9852 (aire=1) |
|
Densidad crítica |
0.227 |
|
Viscosidad a 0ş C |
0,000093 poises |
|
Masa molar |
28,05 g/mol |
|
Punto de fusión |
104 K (-169,15 °C) |
|
Tensión superficial al punto de ebullición |
16,5 dinas/cm |
|
Calor de vaporización al punto de ebullición |
118,5 cal/grs |
|
Punto de ebullición |
169,5 K (-103,65 °C) |
|
Calor de hidrogenación |
32,8 Kcal/mol |
|
Calor de combustión (bruto) |
337,28 Kcal/mol |
|
Temperatura crítica |
282,9 K (9,90ş C) |
|
Presión crítica |
50,7 Atm. |
|
Límite de inflamabilidad en el aire (Min |
3-3,5% |
|
Límite de inflamabilidad en el aire (Max) |
16-29% |
|
Temperatura de autoignición en aire |
490ş C |
|
Propiedades químicas |
|
|
Acidez (pKa) |
44 |
|
Solubilidad en agua |
Miscible |
|
Termoquímica |
|
|
ΔfH0gas |
n/d kJ/mol |
|
ΔfH0líquido |
n/d kJ/mol |
|
S0líquido, 1 bar |
n/d J·mol-1·K-1 |
|
Valores en el SI y en condiciones normales de 0 °C y 1 atm), salvo que se indique lo contrario. |
|
żQué es el etileno?
El etileno o eteno es un compuesto químico orgánico formado por dos átomos de carbono enlazados mediante un doble enlace. Se halla de forma natural en las plantas.
Es el hidrocarburo olefinico o insaturado más sencillo, es el miembro más simple de los alquenos. Es un gas incoloro e inflamable, con olor débil y agradable. Es uno de los productos químicos más importantes de la industria química. Se usa mucho como materia prima en la industria química orgánica sintética.
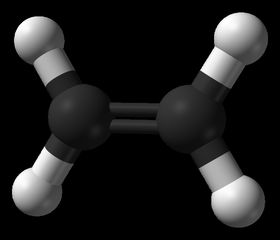
Estructura
La molécula es plana y está formada por cuatro enlaces simples C-H y un enlace doble C=C, que le impide rotar excepto a altas temperaturas.
La molécula no puede rotar alrededor del doble enlace y todos los átomos están en el mismo plano. El ángulo entre los dos enlaces carbono-hidrógeno es de 117ş, muy próximo a los 120ş correspondientes a una hibridación sp2.
Reactividad química
La región del doble enlace es relativamente rica en densidad electrónica (es un centro nucleófilo) y puede reaccionar con electrófilos (con deficiencia de electrones) a través de reacciones de adición. Mediante este tipo de reacciones se pueden sintetizar derivados halogenados.
También se puede adicionar agua (reacción de hidratación) para dar etanol; se emplea un ácido como el ácido sulfúrico o el ácido fosfórico como catalizador. La reacción es reversible.
A altas presiones y con un catalizador metálico (platino, rodio, níquel) se puede hacer reaccionar con hidrógeno molecular para dar etano.
Las reacciones químicas del etileno pueden ser divididas en aquellas que tienen importancia comercial y otras de interés puramente académico. Esta división es necesariamente arbitraria y las reacciones incluidas en la segunda categoría pueden llegar a pertenecer a la primera en el futuro.
Polimerización
La polimerización del etileno representa el segmento más grande de la industria petroquímica con el polietileno ranqueado en el primer lugar como consumidor del etileno. El etileno (99,9 % de pureza), es polimerizado bajo específicas condiciones de temperatura y presión y con la presencia de un iniciador catalítico, generándose una reacción exotérmica.
Oxidación
Las reacciones de oxidación del etileno dan oxido de etilenglicol, acetaldehído y acetato de vinilo; ranqueados segundo, sexto y octavo respectivamente como consumidores de etileno en EEUU. El proceso de oxidación directa es utilizado actualmente en reemplazo del antiguo proceso de oxidación multietapas debido a que es más económico.
Obtención
La mayor parte del etileno producido mundialmente se obtiene por craqueo con vapor (steam cracking) de hidrocarburos de refinería (etano, propano, nafta y gasóleo, principalmente). También se obtiene el etileno a partir del reformado catalítico de naftas o a partir de gas natural (Oxidative Coupling of Methane, OCM).
También puede obtenerse en laboratorios de Química Orgánica mediante la oxidación de Alcoholes.
Biosíntesis
Se produce en casi todos los órganos de las plantas superiores, aunque la tasa de producción dependerá del tipo de tejido y de su estadío de desarrollo. En general las regiones meristemáticas y nodales son las más activas en la biosíntesis. Sin embargo la producción también se incrementa durante la abscisión foliar, senescencia de las flores y maduración de frutos.
Se biosintetiza a partir del aminoácido Metionina, que por acción de una Ado-Met sintasa genera Ado-Met. La etapa limitante en la ruta es la conversión de Ado Met en Ácido-1-aminociclopropanocarboxílico (ACC), catalizado por la ACC sintasa. La última etapa de la vía la cataliza una oxidasa que requiere O2 como sustrato. El grupo CH3-S (tiometilo) de la metionina es reciclado a través del ciclo de Yang nuevamente hasta Metionina; esta vía cíclica involucra el consumo de energía (bajo la forma de ATP) y de O2.
Su biosíntesis está incrementada en plantas expuestas a condiciones ambientales de estrés y en especies terrestres es considerado un signo de injuria asociado con la degradación de la clorofila y la peroxidación de lípidos de membranas. La presencia de jasmonatos favorece su síntesis.
Aplicaciones
El etileno ocupa el segmento más importante de la industria petroquímica y es convertido en una gran cantidad de productos finales e intermedios como plásticos, resinas, fibras y elastómeros (todos ellos polímeros) y solventes, recubrimientos, plastificantes y anticongelantes
La mayor parte del etileno se emplea para la obtención de polímeros. Mediante reacciones de polimerización se obtiene el polietileno de alta densidad y el de baja densidad. También se obtiene dicloroetileno, intermedio para la síntesis de cloruro de vinilo, que se polimeriza a cloruro de polivinilo, y otros hidrocarburos clorados. Además se puede hacer reaccionar con benceno para dar etilbenceno, obteniéndose estireno, que puede polimerizarse dando poliestireno.
Se emplea como producto de partida de otros polímeros, como la síntesis del monómero acetato de vinilo para la obtención de acetato de polivinilo o la síntesis de etilenglicol (a través del intermedio óxido de etileno) que con ácido terftálico da tereftalato de polietileno.
El etileno se utiliza, en combinación con otros hidrocarburos saturados e insaturados, sintetizados a partir del caucho, teniendo estos muchas aplicaciones en la industria. Destaca fundamentalmente el EPDM, Etileno Propileno Dieno Monómero, con el que se obtienen películas de caucho saturado con múltiples aplicaciones en la industria automovilística y de la construcción, por su alta resistencia a las oscilaciones de temperatura, su flexibilidad y su capacidad impermeabilizante.
El etilenglicol también sirve como anticongelante, y el óxido de etileno se puede emplear para la síntesis de algunos éteres glicólicos (para pinturas o tensioactivos) y otros productos.
El etanol se puede obtener mediante la hidratación del etileno y se emplea como combustible o en la síntesis de ésteres etílicos, disolventes, y otros productos. También se puede obtener, a través de la síntesis de propionaldehido, ácido propiónico y alcohol n-propílico. Por oxidación del etileno se obtiene acetaldehido, el cual se emplea en la síntesis de n-butanol y ácido acético.
El etileno, que se encuentra naturalmente en las plantas, también se emplea para provocar la maduración de la fruta. Esto se debe a que se libera un gas, que al entrar en contacto con otros vegetales, ya sea fruta o planta, provoque su precoz maduración, o en el caso de la planta, un envejecimiento prematuro.
Polietileno (PE)
Es un termoplástico que se caracteriza por ser resistente, flexible y poco denso. Como ejemplos de aplicación se pueden nombrar recipientes, tubos flexibles, sogas y películas.
Hay dos clases de Polietileno; el de alta densidad (0,941-0,970 grs/ml) que se usa para tuberías y desagües, especialmente para formas corrugadas de gran diámetro. Y el de baja densidad (0,910-0,940 grs/ml) que se utiliza en la fabricación de películas, cables, alambres y recubrimientos de papel. (Ver más del Polietileno)
Policloruro de vinilo
Se obtiene por adición a partir del cloruro de etileno. Sus principales características son ser resistente, algo elástico y poco desgastable; es por esto que se utiliza en revestimientos de suelos, paredes y tanques, cańos y juntas.
Poliestileno (PS)
Se obtiene a partir de estireno o fenileteno. Se caracteriza por ser transparente y rígido por lo que se lo puede utilizar en inyección, extrusión y piezas termoformadas (envases desechabas, interiores de heladera) y también en aislamientos (expandido).
Poliacrilonitrilo
Se utiliza como monómero el acrilonitrilo o cianoeteno. Es un compuesto fuerte, fácil de teńir y puede hilarse. Estas características lo hacen apto para la fabricación de fibras textiles (orlon, cashmilon, Dralon).
Politetrafloruroeteno (teflón, fluon)Se fabrica a partir de tetrafluoroeteno. Es un polímero muy inerte, no adhesivo y autolubricante, además de su gran resistencia a altas temperaturas. Como ejemplos de su aplicación se pueden nombrar juntas, bujes, y revestimientos de utensilios de cocina. (Ver más del Politetrafloruroeteno)
Oxido de etileno
Es un gas incoloro o un líquido incoloro, movible e inflamable. Se usa mucho como intermedio químico en la fabricación de glicol etilénico, glicoles polietilénicos y sus derivados, etanolaminas, cianhidrina etilénica y detergentes no iónicos. Se usa también como fumigante.
De sus derivados es el óxido propilénico el más importante de los óxidos de alquilenos, y el óxido de estireno el más importante de los derivados aromáticos.
Etileno en las plantas
El etileno es la fitohormona responsable de la maduración de los frutos, además de la senescencia de hojas y flores y de la abscisión del fruto. La famosa frase de que una manzana podrida echa a perder al resto tiene su fundamento científico precisamente en el etileno puesto que, cuando una fruta madura desprende etileno, acelerando la maduración de las frutas que la rodean.
Afecta el crecimiento, desarrollo, maduración y envejecimiento de todas las plantas. Normalmente es producido en cantidades pequeńas por la mayoría de las frutas y vegetales. Muchas frutas producen grandes cantidades de etileno y resulta en una maduración uniforme cuando es expuesta a una fuente externa de etileno.
El etileno, siendo un hidrocarburo, es muy diferente a otras hormonas vegetales naturales. Aunque se ha sabido desde principios de siglo que el etileno provoca respuestas tales como geotropismo y abscisión, no fue sino hasta los ańos 1960s que se empezó a aceptar como una hormona vegetal. Se sabe que el efecto del etileno sobre las plantas y secciones de las plantas varía ampliamente. Ha sido implicado en la maduración, abscisión, senectud, dormancia, floración y otras respuestas. El etileno parece ser producido esencialmente por todas las partes vivas de las plantas superiores, y la tasa varía con el órgano y tejido específicos y su estado de crecimiento y desarrollo. Las tasas de síntesis varían desde rangos muy bajos (0.04-0.05 µl/kg-hr) en blueberries (Vaccinium spp.) a extremadamente elevadas (3,400 µl/kg-hr) en flores desvanecientes de orquídeas Vanda. Se ha encontrado que las alteraciones en la tasa sintética de etileno están asociadas cercanamente al desarrollo de ciertas respuestas fisiológicas en plantas y sus secciones, por ejemplo, la maduración de frutas climatéricas y la senectud de flores.
Ya que el etileno está siendo producido continuamente por las células vegetales, debe de existir algún mecanismo que prevenga la acumulación de la hormona dentro del tejido. A diferencia de otras hormonas, el etileno gaseoso se difunde fácilmente fuera de la planta. Esta emanación pasiva del etileno fuera de la planta parece ser la principal forma de eliminar la hormona. Técnicas como la ventilación y las condiciones hipobáricas ayudan a facilitar este fenómeno durante el periodo poscosecha al mantener un gradiente de difusión elevado entre el interior del producto y el medio que lo rodea. Un sistema de emanación pasivo de esta naturaleza implicaría que la concentración interna de etileno se controla principalmente por la tasa de síntesis en lugar de la tasa de remoción de la hormona.
Efectos fisiológicos
-
Promueve la maduración de frutos. Por aumento en los niveles de enzimas hidrolíticas que ablandan el tejido, producen la hidrólisis de los productos almacenados, incrementan la velocidad de respiración y la pigmentación de los frutos.
-
Favorecen la epinastia de hojas. La epinastia es la curvatura hacia abajo de las hojas debido a que el lado superior del pecíolo (adaxial) crece más rápido que el inferior (abaxial).
-
Induce la expansión celular lateral. Por reordenamiento de las fibras de celulosa en la pared, que cambian hacia una orientación longitudinal.
-
Pone fin a la dormancia de los brotes.
-
Inicia la germinación de semillas.
-
Inhibe el crecimiento de la raíz y favorece la formación de raíces adventicias.
-
Favorece la senescencia de las hojas: efecto en el que se involucra un balance hormonal con las citocininas.
-
Favorecen la abscisión de hojas y frutos. Es el principal regulador de la abscisión. El etileno estimula la abscisión de hojas y frutos al aumentar la síntesis y secreción de enzimas que degradan la pared celular tales como celulasas y pectinasas. En este proceso esta involucrado un balance hormonal con las auxinas.
Mecanismo de acción
El receptor de etileno se denomina ETR1; En Arabidopsis thaliana es un dímero de 2 proteínas integrales de membrana, con actividad histidina kinasa y capacidad autofosforilante. La unión del etileno a su receptor induce su autofosforilación a nivel de residuos de histidina y luego transferencia de estos fosfatos hacia residuos de aspartato. El receptor así activado inicia una cascada de seńalizaciones hacia otras proteínas efectoras (cascada del tipo MAP Kinasa, con destino final a nivel del DNA).
La unión del etileno al receptor da como resultado la inactivación de un regulador negativo CTR 1 (que se hallaba inhibiendo a la proteína transmembrana EIN 2) por lo que la proteína EIN 2 cobra actividad, funcionando como un canal de iones (probablemente iones Ca+2), lo que se traduce en una posterior activación del factor de transcripción EIN 3, que actúa a nivel genómico induciendo la expresión genética de proteínas efectoras.
Catabolismo
Difusión hacia la atmósfera circundante, o bien oxidación hasta etilenóxido, etilenglicol o CO2. Como es fácilmente oxidado a etilenglicol por acción del permanganato de potasio, se aprovecha esta propiedad en horticultura. Las frutas o flores empacadas en cajones son cubiertas con alúmina o silicagel impregnada en KMnO4 para remover el etileno que se forma y así disminuir la velocidad de maduración.
Transporte
Se transporta de célula a célula en el simplasto y floema, difundiendo en el citosol, ya que es suficientemente soluble en agua para ser transportado en soluciones y suficientemente no polar para pasar a través de las membranas rápidamente. El sitio de acción del etileno es próximo al sitio de síntesis.
Etileno en la maduración de los frutos
El etileno es un compuesto químico relacionado con la maduración y su exclusión se traduce en un retraso de dicho proceso fisiológico.
Los azúcares y otros componentes sufren alteraciones importantes y se forma anhídrido carbónico (CO2) y agua.
Los fenómenos destacados que tienen lugar durante la maduración de las frutas son la respiración, el endulzamiento, el ablandamiento, los cambios en el aroma, la coloración y el valor nutritivo. Y todos estos procesos influyen notablemente en la resistencia y buena presencia de las frutas durante el almacenamiento, el transporte y la comercialización de las mismas.
Durante la respiración de las frutas se forma un compuesto gaseoso llamado etileno. Este compuesto acelera los procesos de maduración, por lo que es preciso evitar su acumulación mediante ventilación de las frutas almacenadas, a fin de aumentar el periodo de conservación de las frutas.
Si este compuesto gaseoso, producido por una fruta madura, se acumula en las cercanías de frutas no maduras, desencadena rápidamente su maduración, lo que contribuye a acelerar el deterioro de todas las frutas.
Las concentraciones de etileno requeridas para la maduración varían según las especies, pero en la mayoría de los casos oscila entre 0.1 a 1 partes por millón.
El etileno como estimulante de la maduración en los frutos de las plantas
El etileno es un gas producido naturalmente por las frutas durante la maduración. En general, estimula los cambios en el color de la piel (ej: tomate, pimiento, platano) o cáscara (ej: cítricos, banana), produce ablandamiento (ej: plátano, tomate) y en algunos casos, mejoras en el sabor (ej: banana, plátano).
Cuando se conocieron los efectos que el etileno tiene sobre la maduración, se comenzó a utilizarlo en tratamientos artificiales para anticipar la recolección de frutas. Se cosecha con un mínimo grado de madurez y mediante la aplicación de este gas, se trata de provocar los mismos cambios que se producirían naturalmente si permanecieran los frutos aún en la planta.
En Estados Unidos es una práctica usual que se cosechen tomates en un estado capaz de madurar separado de la planta (de color verde pero fisiológicamente maduros), se trasladen de una costa a la otra del país en camiones y se traten con etileno al llegar a destino. De esta manera se alcanza el color deseado por el comprador, se obtiene un producto uniforme y se evitan las pérdidas por sobremadurez y podredumbres.
Algunos frutos cítricos, dependiendo de la especie, variedad, sistema de cultivo y condiciones climáticas, pueden alcanzar la madurez y aún mantener la cáscara verde. Es importante dejar en claro que si los frutos no están maduros también se desverdizarán pero no mejorarán su sabor con el tratamiento.
Los frutos cítricos liberan bajos niveles de etileno durante su desarrollo en la planta pero responden en general al tratamiento con este gas en la postcosecha, aunque sólo tiene efecto sobre el cambio de color de la cáscara (desverdizado). El desverdizado es una práctica imprescindible y muy utilizada en situaciones en que naturalmente no se alcanza el color deseado en la planta, generalmente por falta de bajas temperaturas.
Para obtener un producto comercialmente aceptable, la fruta cítrica debe cosecharse con un mínimo grado de madurez, debiéndose tomar en cuenta el porcentaje de jugo y el valor de ratio o relación sólidos solubles / acidez del jugo. Es decir, alcanzado los valores mínimos de los índices de cosecha establecidos, se puede iniciar la recolección y forzarse el cambio de color del verde al amarillo (limones), o anaranjado (naranjas y mandarinas) para enviar el producto ya acondicionado al mercado local o de exportación.
En esa misma línea, el uso de etileno también puede ser beneficioso para provocar el cambio de color del verde al rojo en pimientos, aunque es importante recalcar que también deben tener un grado de madurez adecuado para que haya respuesta. Los pimientos completamente verdes no están preparados para responder a la presencia de etileno, pero sí aquellos que han iniciado el cambio de color (pueden presentar pequeńas vetas de color amarronado o amarillo-anaranjado en la piel).
Para realizar los tratamientos artificiales con etileno se requiere contar con una cámara o habitación que pueda mantenerse cerrada lo más herméticamente posible y en la cual pueda hacerse un control de la temperatura y humedad.
En general, se necesita mantener una temperatura de 18-21°C y 85-90% de humedad relativa. El etileno puede ser aplicado utilizando generadores (en los que se libera el gas por calentamiento de un líquido) o como gas puro o en mezcla con oxígeno, a partir de cilindros.
El tiempo de tratamiento puede ser de 24, 48 a 72 horas, dependiendo del tipo de fruta y de su grado de madurez de cosecha. También se debe contar con una adecuada circulación dentro de la cámara y realizar recambios de aire con una frecuencia regular para evitar la acumulación de dióxido de carbono.
Documentación
http://www.biologia.edu.ar
http://www.catalyticgenerators.com/
http://www.consumer.es
http://www.efn.uncor.edu
http://es.scribd.com/
http://es.wikipedia.org/
http://www.telecable.es/personales/albatros1
http://www.textoscientificos.com